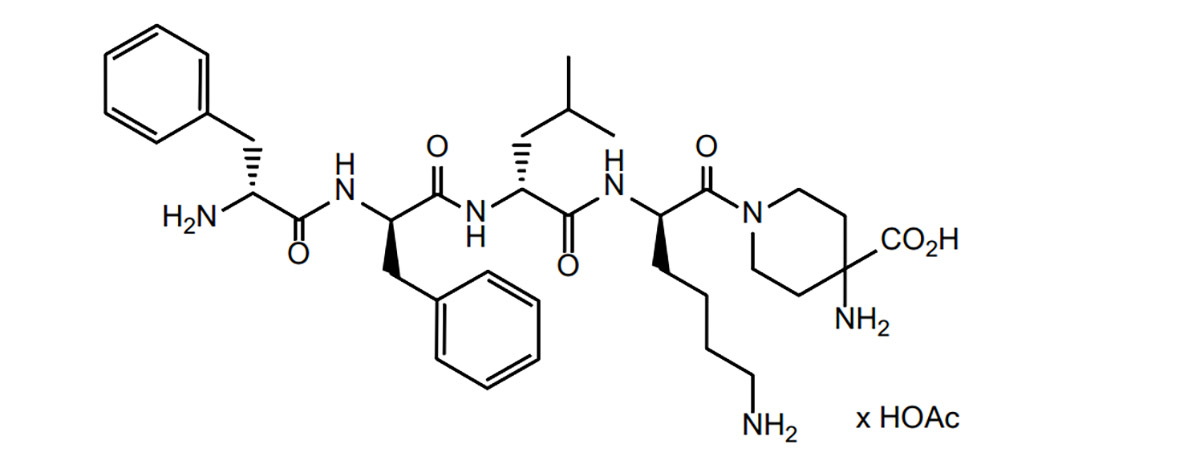
כבר ב-24 באוגוסט 2021, Cara Therapeutics ושותפתה העסקית Vifor Pharma הודיעו כי האגוניסט הראשון מסוגו לקולטן אופיואידים קאפה, דיפלייקפאלין (KORSUVA™), אושר על ידי ה-FDA לטיפול בחולי מחלת כליות כרונית (CKD) (גירוד בינוני/חמור חיובי עם טיפול המודיאליזה), והושק צפוי ברבעון הראשון של 2022. Cara ו-Vifor חתמו על הסכם רישיון בלעדי למסחור KORSUVA™ בארצות הברית והסכימו למכור את KORSUVA™ ל-Fresenius Medical. ביניהן, Cara ו-Vifor מחזיקות כל אחת ב-60% ו-40% ברווחים מהמכירות שאינן Fresenius Medical; לכל אחת מהן יש 50% ברווחים מהמכירות של Fresenius Medical.
גירוד הקשור למחלת כליות כרונית (CKD-aP) הוא גירוד כללי המופיע בתדירות ובעוצמה גבוהות בחולי CKD שעוברים דיאליזה. גירוד מופיע בכ-60%-70% מהחולים המקבלים דיאליזה, מתוכם 30%-40% סובלים מגירוד בינוני/חמור, המשפיע קשות על איכות החיים (למשל, איכות שינה ירודה) וקשור לדיכאון. אין טיפול יעיל לגירוד הקשור למחלת כליות כרונית בעבר, ואישור דיפלייקפאלין מסייע להתמודד עם פער העצום בצורך הרפואי. אישור זה מבוסס על שני ניסויים קליניים מרכזיים בשלב III שהוגשו ל-NDA: נתונים חיוביים מניסויי KALM-1 ו-KALM-2 בארה"ב ובעולם, ונתונים תומכים מ-32 מחקרים קליניים נוספים, המדגימים כי KORSUVA™ נסבל היטב.
לא מזמן, הגיעו חדשות טובות מהמחקר הקליני של דיפליקפלין ביפן: ב-10-1-2022, קארה הודיעה ששותפותיה, מארוישי פארמה ו-קיסי פארמה, אישרו כי זריקת דיפליקפלין משמשת ביפן לטיפול בגרד בחולי המודיאליזה. ניסויים קליניים שלב III: נקודת הסיום העיקרית הושגה. 178 חולים קיבלו 6 שבועות של דיפליקפלין או פלצבו והשתתפו במחקר הרחבה פתוח בן 52 שבועות. נקודת הסיום העיקרית (שינוי בציון סולם הדירוג המספרי של הגרד) ונקודת הסיום המשנית (שינוי בציון הגירוד בסולם החומרה של שיראטורי) השתפרו משמעותית מתחילת המחקר בקבוצת הדיפליקפלין בהשוואה לקבוצת הפלצבו ונסבלו היטב.
דיפליקפאלין הוא סוג של פפטידים אופיואידים. בהתבסס על כך, מכון המחקר פפטידים חקר את הספרות על פפטידים אופיואידים, וסיכם את הקשיים והאסטרטגיות של פפטידים אופיואידים בפיתוח תרופות, כמו גם את מצב פיתוח התרופות הנוכחי.
זמן פרסום: 17 בפברואר 2022