אינדיקציה (שימוש מאושר): בשנת 2019, אישר אותו ה-FDA לטיפול בהפרעת חשק מיני היפואקטיבית מוכללת נרכשת (HSDD) אצל נשים לפני גיל המעבר, כאשר המצב גורם למצוקה ניכרת ואינו נובע ממצבים רפואיים/פסיכיאטריים אחרים או מתופעות לוואי של תרופות.
מנגנון הפעולה
PT-141 הוא אגוניסט של קולטן מלנוקורטין (בעיקר קולטן MC4) אשר מווסת את התשוקה המינית דרך מסלולים של מערכת העצבים המרכזית.
בניגוד למעכבי PDE5 (למשל, סילדנפיל), המשפיעים בעיקר על כלי הדם, PT-141 פועל באופן מרכזי כדי להשפיע על מוטיבציה מינית ועוררות.
פרמקולוגיה ומינון
מתן: הזרקה תת עורית, לפי הצורך (לפי דרישה).
מינון מאושר: 1.75 מ"ג תחת הזרקה
פרמקוקינטיקה:
Tmax ≈ ~60 דקות
t½ ≈ 2-3 שעות
ההשפעות יכולות להימשך מספר שעות, בדיווחים מסוימים עד כ-16 שעות.
יעילות קלינית (ניסויי שלב III - RECONNECT, 24 שבועות, ניסויים קליניים מבוקרים ואקראיים)
נקודות סיום ראשוניות:
מדד תפקוד מיני נשי - תחום תשוקה (FSFI-D)
סולם מצוקה מינית נשית (FSDS-DAO)
תוצאות עיקריות (מחקרים מקובצים 301 + 302):
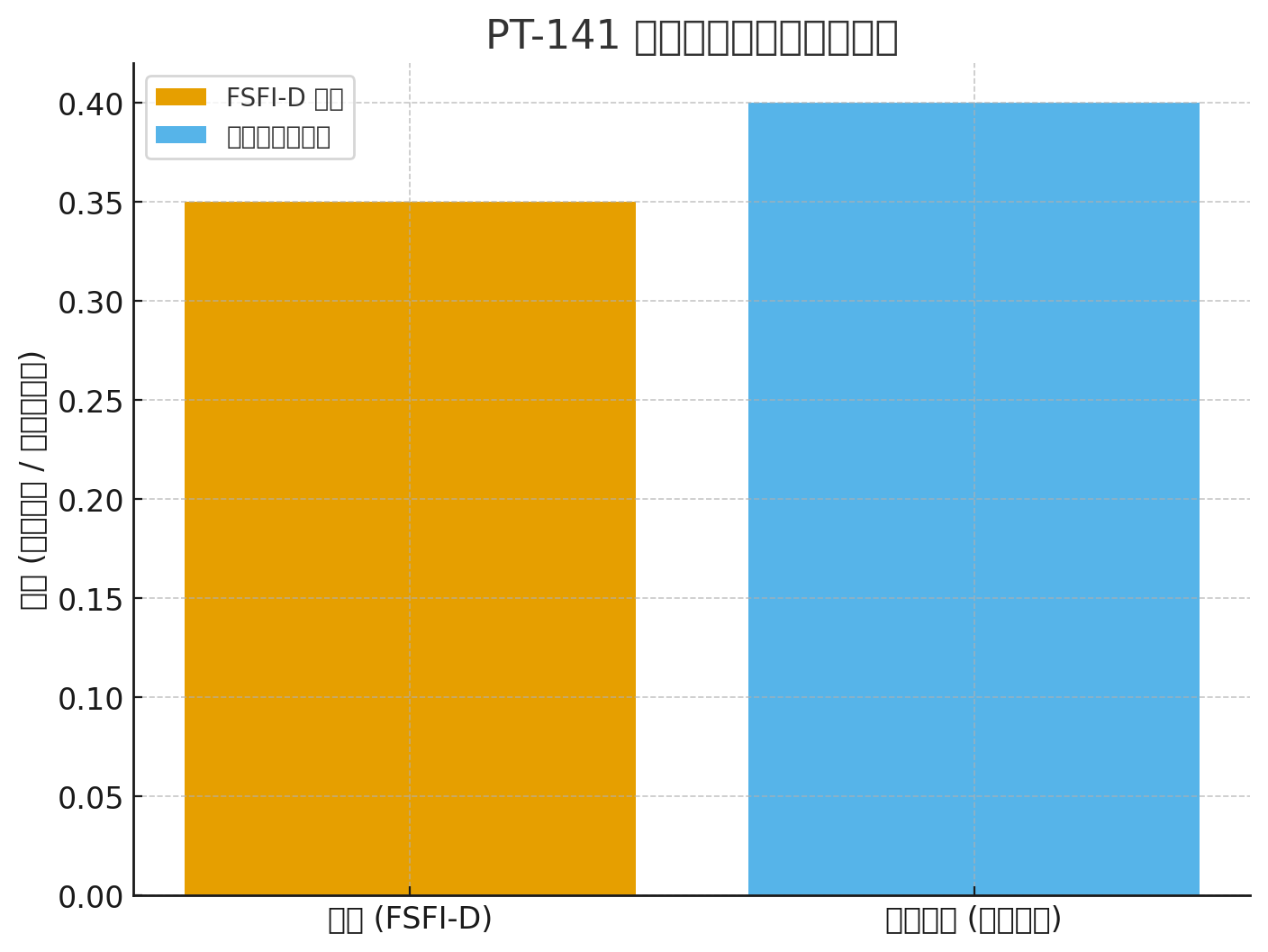
שיפור ב-FSFI-D: +0.35 לעומת פלצבו (P<0.001)
ירידה בציון FSDS-DAO: −0.33 לעומת פלצבו (P<0.001)
נקודות סיום נוספות: תוצאים תומכים (ציוני תפקוד מיני, שביעות רצון מדווחת על ידי המטופלים) היו במגמת חיובית, אך אירועים מיניים מספקים (SSEs) לא תמיד הראו הבדלים משמעותיים עקביים.
תופעות לוואי (המדווחות בתדירות הגבוהה ביותר בניסויים)
שכיח (≥10%):
בחילות (~30-40%; עד ~40% דווחו בניסויים)
שטיפה (≥10%)
כאב ראש (≥10%)
השפעות קרדיווסקולריות:
נצפו עלייה חולפת בלחץ הדם ושינויים בקצב הלב, שבדרך כלל חולפים תוך מספר שעות.
התווית נגד או יש להשתמש בזהירות בחולים עם יתר לחץ דם בלתי מבוקר או מחלות לב וכלי דם.
כבד: דיווחים נדירים על עליות חולפות ברמות אנזימי כבד; דיווחי מקרים נדירים ביותר מצביעים על פגיעה כבדית חריפה אפשרית, אך לא שכיחים.
בטיחות לטווח ארוך (מחקר הרחבה)
מחקר פתוח בן 52 שבועות מצא שיפורים מתמשכים בתשוקה ללא אותות בטיחות חדשים משמעותיים.
פרופיל הבטיחות לטווח ארוך נחשב נסבל היטב באופן כללי, כאשר בעיות הסבילות העיקריות עדיין הן תופעות לוואי לטווח קצר כמו בחילות.
הערות שימוש מרכזיות
האוכלוסייה המאושרת מוגבלת: רק לנשים לפני גיל המעבר עם HSDD נרכש וכללי.
לא מאושר באופן נרחב לגברים (איבוד ערמונית או תשוקה נמוכה אצל גברים נותרו במחקר).
בדיקות בטיחות הן קריטיות: יש להעריך יתר לחץ דם, מחלות לב וכלי דם והיסטוריה כבדית לפני מתן מרשם.
סיכום נתונים מהיר
אישור ה-FDA: 2019 (Vyleesi).
מינון: הזרקה תת עורית של 1.75 מ"ג, לפי דרישה.
PK: Tmax ~60 דקות; t½ 2-3 שעות; השפעות עד ~16 שעות.
יעילות (שלב III, מאוחד):
FSFI-D: +0.35 (P<.001)
FSDS-DAO: −0.33 (P<.001)
אירועים שליליים:
בחילות: עד ~40%
שטיפה: ≥10%
כאב ראש: ≥10%
נצפתה עלייה חולפת בלחץ הדם.
טבלה וגרף השוואתיים (סיכום)
| סוג מחקר / נתונים | נקודת קצה / מדידה | ערך / תיאור |
|---|---|---|
| שלב ג' (301+302 מאוחדים) | FSFI-D (תחום הרצון) | +0.35 לעומת פלצבו (P<0.001); FSDS-DAO -0.33 |
| אירועים שליליים | בחילה, הסמקה, כאב ראש | בחילות ~30-40% (מקסימום ~40%); הסמקה ≥10%; כאב ראש ≥10% |
זמן פרסום: 30 בספטמבר 2025